Estudo revela que teste rápido para Covid-19 criado na UFPR é mais preciso e rápido que padrão ouro
Pesquisadores do Laboratório de Microbiologia Molecular da Universidade Federal do Paraná (UFPR), Setor Litoral, compararam a performance do teste imunológico para a Covid-19 desenvolvido pela equipe com a do teste Elisa tradicional (Enzyme-Linked Immunosorbent Assay), considerado padrão ouro para ensaios imunológicos. A conclusão foi de que o método paranaense é mais preciso e mais rápido. Além disso, o estudo revela que a nova tecnologia tem potencial para ser utilizada em pontos de atendimento de saúde e pode ser adaptada para o diagnóstico de outras doenças. O coordenador do Laboratório, professor Luciano Fernandes Huergo, é responsável por conduzir a pesquisa.
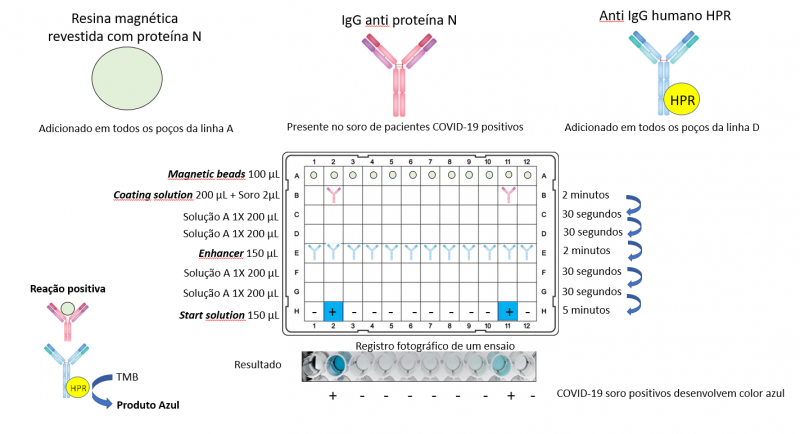
O teste criado pelos cientistas da UFPR é uma adaptação do método Elisa tradicional. A diferença é que em vez de o processo ocorrer na superfície de uma placa de plástico, ele acontece em nanopartículas magnéticas revestidas com antígenos virais. A técnica permite a redução no tempo de reação (interação entre antígeno e anticorpo) proporcionando um procedimento mais rápido. Enquanto o Elisa tradicional leva cerca de três horas para apresentar o resultado, o novo método precisa de apenas 12 minutos e pode ser adaptado para testar até 96 amostras simultâneas, com o auxílio de sistemas robotizados disponíveis comercialmente, mantendo esse tempo para o resultado.
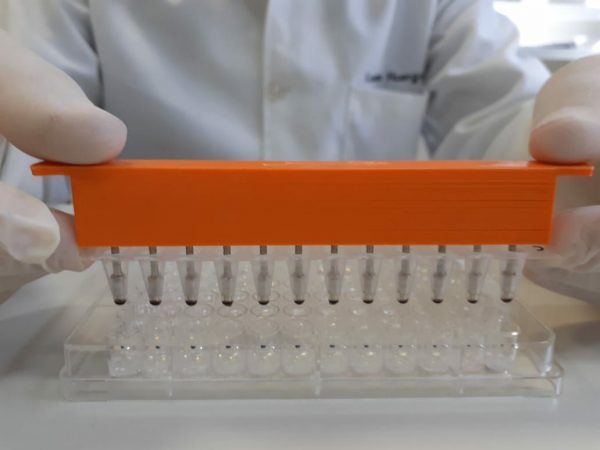
O processo acontece em nanopartículas magnéticas revestidas com antígenos virais. Foto: Laboratório de Microbiologia Molecular
Como funciona
Para a realização do teste, é necessário um volume muito baixo de sangue, que pode ser coletado com uma lanceta igual à utilizada para o exame de glicose. São necessários apenas dois microlitros de fração solúvel, conhecida como soro, também sendo possível utilizar o sangue bruto do paciente.
Essa amostra é incubada com os antígenos virais que estão mobilizados na superfície de nanopartículas magnéticas. Após cerca de dois minutos nessa fase, são feitas etapas de lavagens e, em seguida, acrescenta-se um revelador, que é o responsável por alterar a cor do material caso haja reação positiva. Assim, se o paciente tiver desenvolvido anticorpos contra o coronavírus, a amostra apresentará uma coloração indicando o resultado positivo.
Geralmente, os anticorpos contra o novo coronavírus (SARS-CoV-2) atingem uma estabilização entre 11 a 16 dias após o início dos sintomas. No entanto, alguns pacientes produzem anticorpos detectáveis já entre dois a quatro dias após os primeiros sinais da doença. Por isso, esses testes imunológicos podem ser úteis como ferramentas adicionais para identificar pacientes na fase aguda da Covid-19 ou os que testaram como falso negativo no exame PCR. “A grande vantagem em relação ao teste rápido tradicional de imunocromatografia é que o resultado da cor no teste da UFPR é diretamente proporcional à quantidade de anticorpos. Ou seja, o ensaio fornece dados da quantidade de anticorpos e não apenas da presença ou ausência, como é o caso do teste rápido tradicional”, revela Huergo.
Comparação e metodologia
Para comprovar a eficiência do novo teste, os pesquisadores coletaram amostras de pacientes do Complexo Hospital de Clínicas (CHC) da UFPR que tiveram a Covid-19 confirmada por PCR. As amostras negativas foram obtidas no banco de doadores do hospital a partir do sangue coletado de indivíduos saudáveis em 2018.
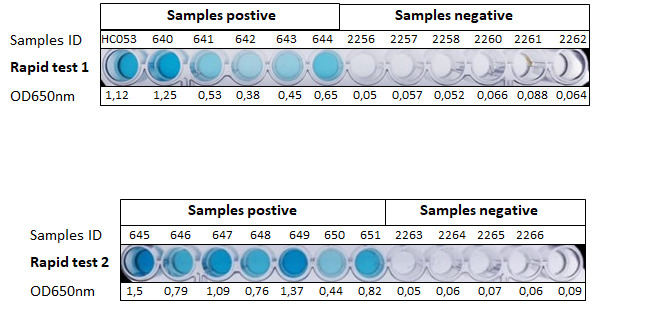
O material colhido passou tanto pelo teste Elisa tradicional quanto pelo método criado na UFPR. De acordo com Huergo, no Elisa regular os testes dos pacientes positivos para Covid-19 mostraram forte reação com os antígenos, enquanto os negativos apresentaram uma pequena reação cruzada. Já na tecnologia baseada em nanopartículas magnéticas, os soros positivos mostraram forte reação com os antígenos e os negativos não apresentaram reação cruzada detectável. A comparação pode ser vista na imagem:
“O nosso teste teve um desempenho melhor do que o Elisa clássico, especialmente para amostras com baixo título de anticorpos. O método classificou corretamente 49 das 50 amostras positivas de Covid-19 testadas e mostrou que não houve falsos positivos nas mais de 140 amostras negativas analisadas”, conta o professor. Apesar de uma maior precisão ser obtida com o uso de um leitor de microplaca, os resultados positivos e negativos podem ser observados por inspeção visual, sem a necessidade de instrumentação.
Após uma revisão recente de diferentes técnicas sorológicas para o diagnóstico da doença, os pesquisadores concluíram que todos os métodos descritos exigiram muito mais tempo para fornecer resultados do que a tecnologia desenvolvida por eles. “Na literatura não há registros de um teste rápido imunológico para Covid-19 que forneça dados quantitativos tão rápido, com alta acurácia e com baixo custo. Acreditamos que a técnica possa representar um novo marco em testes imunológicos e que em breve deva substituir o Elisa tradicional, que já é empregado desde os anos 70 quando foi descrito pela primeira vez”, avalia Huergo.
Vantagens
Para a equipe de cientistas, o teste criado por eles tem muitas vantagens com relação ao teste imunológico padrão ouro utilizado atualmente. A primeira delas está associada à quantidade de material necessário para a análise: apenas de uma gota contendo dois microlitros de soro. É possível, ainda, utilizar o sangue total, ou seja, sem precisar passar pela etapa de separação da parte solúvel do sangue.
As reações podem ser interpretadas por inspeção visual, o que facilita a análise em pontos de atendimento, não sendo necessário levar para laboratório nem instrumentação específica. O tempo total de reação é 15 vezes menor que o do teste clássico, resultando em um exame muito mais rápido, que leva 12 minutos no total e pode processar centenas de amostras em poucas horas.
O antígeno, criado no laboratório da equipe, pode ser reproduzido em larga escala, sem a necessidade de instrumentação laboratorial sofisticada e com um custo muito baixo. Isso barateia o valor do teste, cujos insumos para produção devem custar aproximadamente R$5,00.
“Acreditamos que o método barato, rápido e quantitativo para detectar anticorpos humanos contra o SARS-CoV-2 descrito neste estudo pode ajudar a rastrear casos de Covid-19, especialmente em países em desenvolvimento como o Brasil. O ensaio requer instrumentação mínima em todas as fases da produção e está pronto para ser avaliado com maior número de amostras, bem como para produção em massa”, defende o pesquisador.
A tecnologia – que está disponível para parcerias de Pesquisa, Desenvolvimento e Inovação (PD&I) e para transferência de tecnologia via Agência de Inovação UFPR – já teve o registro de patente depositado. Os cientistas estão em busca de parceiros para que a produção seja feita em grande escala.
Leia mais sobre a tecnologia desenvolvida pelo Laboratório de Microbiologia Molecular da UFPR
Covid-19: pesquisa da UFPR Litoral aponta avanços para testes imunológicos
Saiba tudo sobre as ações da UFPR relacionadas ao novo coronavírus